-
Упражнение по ОВР (окислительно-восстановительные реакции)
Можно любой вариант.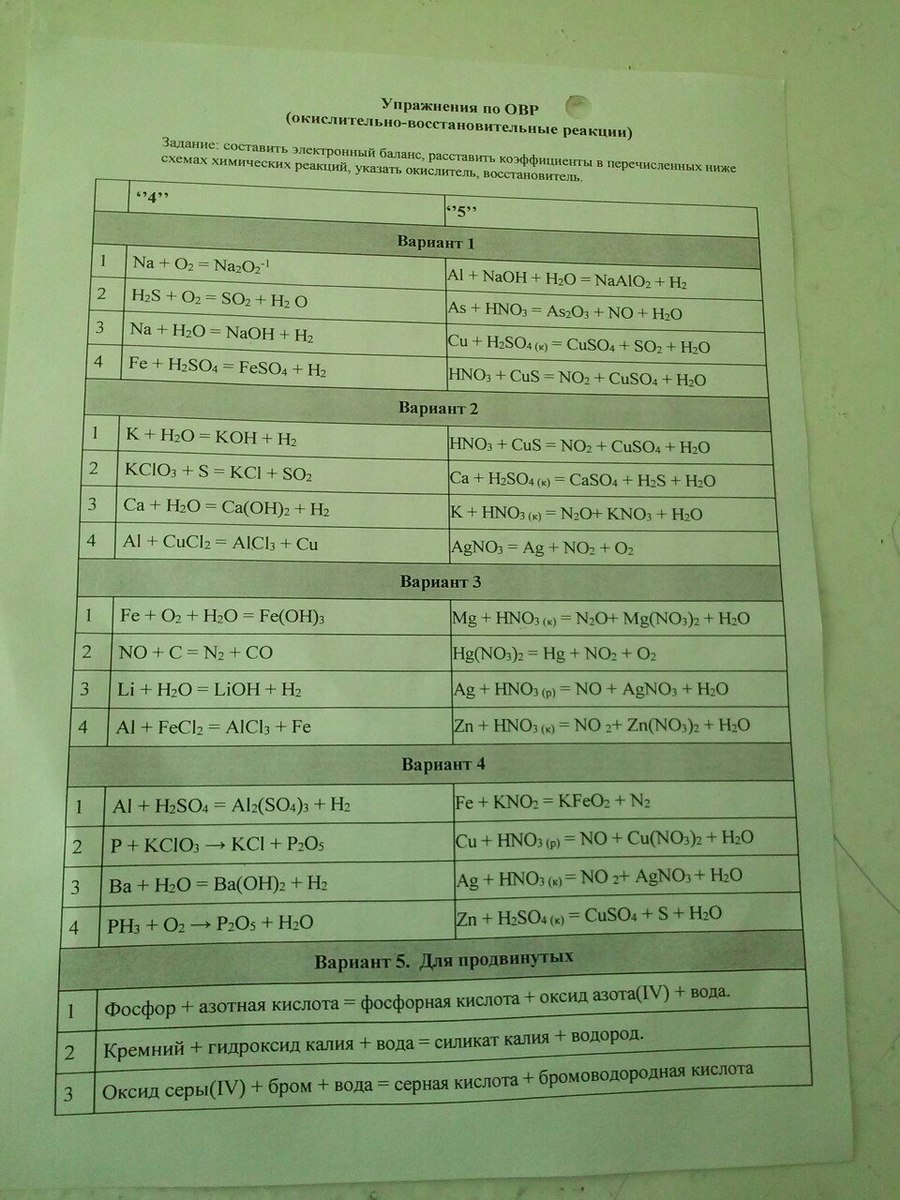
Ответы 1
-
Вариант 21) K⁰ + H₂⁺O →K⁺OH + H₂⁰ K⁰ - e⁻→ K⁺ восстановитель, процесс окисленияH⁺ + e⁻ → H⁰ окислитель, процесс восстановления2K + 2H₂O = 2KOH + H₂2) KCI⁺⁵O₃ + S⁰ → KCI⁻ + S⁺⁴O₂ CI⁺⁵ +6e⁻ → CI⁻ 6 2 окислитель, процесс восстановления 12S⁰ - 4e⁻→ S⁺⁴ 4 3 восстановитель, процесс окисления 2KCIO₃ + 3S = 2KCI + 3SO₂ 3) Ca⁰ + H₂⁺O → Ca⁺²(OH)₂ + H₂⁰ Ca⁰ - 2e⁻ → Ca⁺² 2 1восстановитель, процесс окисления 2 H⁺ +e⁻ → H⁰ 1 2 окислитель, процесс восстановления Ca + 2H₂O = Ca(OH)₂ + H₂4) AI⁰ + Cu⁺²CI₂ → AI⁺³CI₃ + Cu⁰AI⁰ -3e⁻ → AI⁺³ 3 2восстановитель, процесс окисления 6Cu⁺² +2e⁻ →Cu⁰ 2 3 окислитель, процесс восстановления 2AI + 3CuCI₂ = 2AICI₃ + 3Cuна "5"1)HN⁺⁵O₃ + CuS⁻² → N⁺⁴O₂ +CuS⁺⁶O₄ + H₂ON⁺⁵ +1e⁻ → N⁺⁴ 1 8 окислитель, процесс восстановления 8S⁻² - 8e⁻→ S⁺⁶ 8 1 восстановитель, процесс окисления 8HNO₃ + CuS = 8NO₂ + CuSO₄ + 4H₂O2) Ca⁰ + H₂S⁺⁶O₄(к) → Ca⁺²SO₄ + H₂S⁻² + H₂OCa⁰ -2e⁻ → Ca⁺² 2 4восстановитель, процесс окисления 8S⁺⁶ +8e⁻ → S⁻² 8 1окислитель, процесс восстановления 4Ca + 5H₂SO₄(к) = 4CaSO₄ + H₂S + 4H₂O3) K⁰ + HN⁺⁵O₃(к) →N⁻³H₄NO₃ + K⁺NO₃ + H₂OK⁰ - e⁻ → K⁺ 1 8 восстановитель, процесс окисления 8N⁺⁵ + 8e⁻ → N⁻³ 8 1окислитель, процесс восстановления 8K + 10HNO₃(к) = N⁻³H₄NO₃ + 8K⁺NO₃ + 3H₂O4) Ag⁺N⁺⁵O₃⁻² →Ag⁰ + N⁺⁴O₂ + O₂⁰Ag⁺ + e⁻ →Ag⁰ 1N⁺⁵ + e⁻ → N⁺⁴ 1 1 окислители, процесс восстановления 2O₃⁻² - 2e⁻ → O₂⁰ 2 1 восстановитель, процесс окисления 2AgNO₃ = 2Ag + 2NO₂ + O₂
-
Автор:
maya37 - 6 лет назад
-
0
-
-
Добавить свой ответ
Еще вопросы
-
помогите решить
2x^2+3x-3=x^2-3x+(-2+x^2) -
слово питають звукова схема
-
Предмет:
Українська мова -
Автор:
mariyahmoon - 6 лет назад
-
Ответов:
1 -
Смотреть
-
-
2x-1\4.5=2.8\4.2 нужно решение
-
Предмет:
Математика -
Автор:
wags - 6 лет назад
-
Ответов:
1 -
Смотреть
-
-
1)Укажите группу слов, в которых все согласные твердые.Объясните свой выбор.
1.Модель, компьютер, интервью,антенна,термос,тембр.
2.Чудо,частушка,щука,район,поют,овощ.
3.Мыши, розы,паращют,цирк,живот,шоссе.
4.Блюдо,резьба,столяр,территория,параллель,черешня.
2)Выпишите слова с мягкими согласными, подчеркните буквы,которые обозначают их мягкость.
3)В каких словах есть отступление от общего правила обозначения мягкости на письме?-
Предмет:
Русский язык -
Автор:
jaliyahmckenzie - 6 лет назад
-
Ответов:
5 -
Смотреть
-
How much to ban the user?
1 hour
1 day
100 years
