-
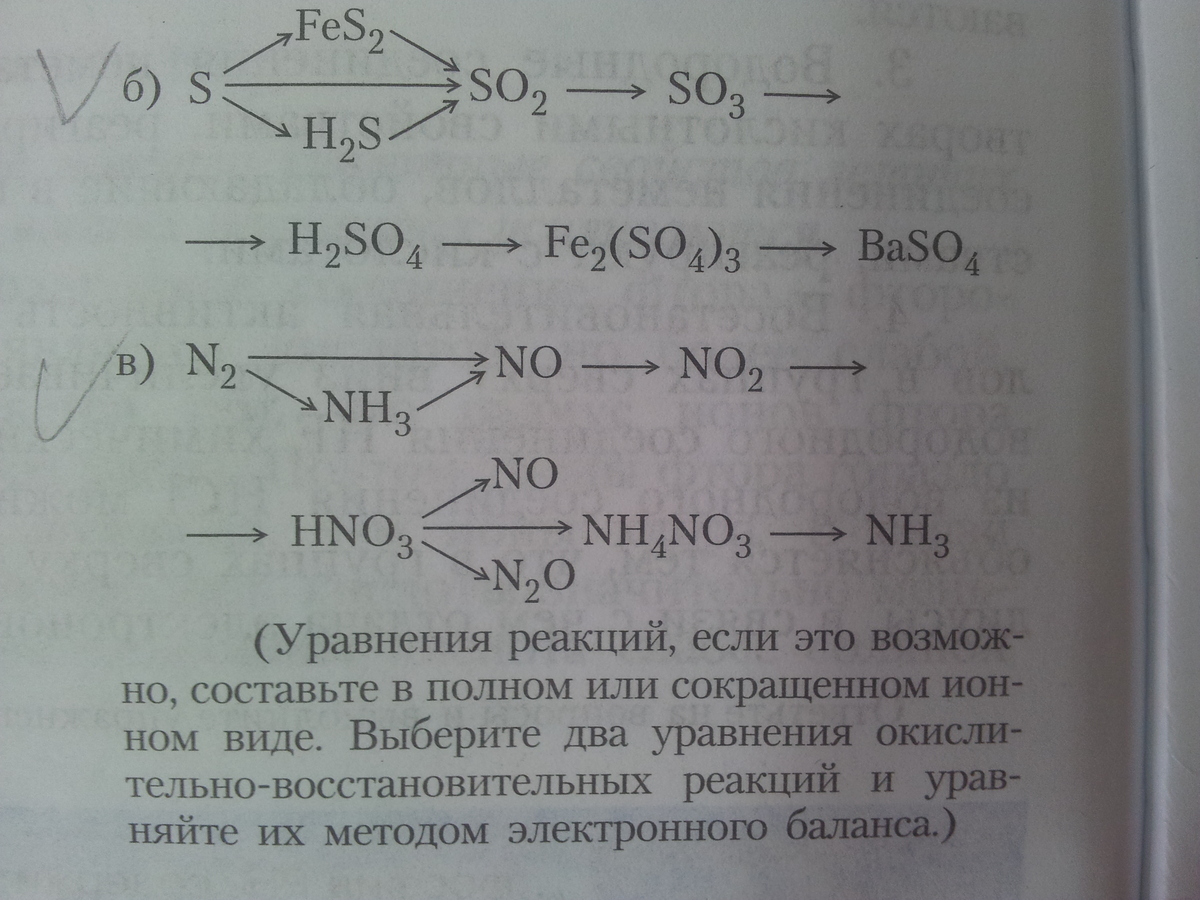
Составьте уравнение реакций, при помощи которых можно осуществить следующие превращения:
Ответы 1
-
1)
S + Fe = FeS
4FeS + 11O2 = 8SO2 + 2Fe2O3
2SO2 + O2 = 2SO3
SO3 + H2O = H2SO4
3H2SO4 + 2FeCl3 = Fe2(SO4)3 + 6HCl
Fe2(SO4)3 + 3BaCl2 = 3BaSO4 + 2FeCl3
S + H2 = H2S
2H2S + 3O2 = 2H2O + 2SO2
2) N2 + O2 = 2NO
2NO + O2 = 2NO2
4NO2 + O2 + 2H2O = 4HNO3
4HNO3 (разб) + 3Ag = 3AgNO3 + NO + 2H2O
HNO3 + NH4OH = NH4NO3 + H2O
NH4NO3 + KOH = KNO3 + NH3 + H2O
10HNO3 (конц) + 8Na = 8NaNO3 + N2O + 5H2O
N2 + 3H2 = 2NH3
4NH3 + 5O2 = 4NO + 6H2O
Ионные уравнения:
Fe2(SO4)3 + 3BaCl2 = 3BaSO4 + 2FeCl3
2Fe[3+] + 3SO4[2-]+ 3Ba[2+] + 6Cl[-] = 3BaSO4 ↓ + 2Fe[3+] + 6Cl[-]
3Ba[2+] + 3SO4[2-] = 3BaSO4 ↓
3H2SO4 + 2FeCl3 = Fe2(SO4)3 + 6HCl
6H[+]+ 3SO4[2-] + 2Fe[3+] + 6Cl[-] = 2Fe[3+] +3SO4[2-] + 6H[+]+ 6Cl[-]
Реакция идет не до конца
примечание: в квадратных скобках, например [2+] - дан заряд ионов
ОВР:
4NH3 + 5O2 = 4NO + 6H2O
1| N[-3] -5e = N[+2] | восстановитель, окисление
2| O2[0] +4e = 2O[-2] | окислитель. восстановление
примечание: в квадратных скобках, например [-2] - дана степень окисления атома
N2 + 3H2 = 2NH3
3| H2[0] -2e = 2H[+1] | восстановитель, окисление
2| N2[0] +3e = 2N[-3] | окислитель. восстановление
примечание: в квадратных скобках, например [-2] - дана степень окисления атома
P.S. удачи!!!!
-
Автор:
cobweb - 6 лет назад
-
0
-
-
Добавить свой ответ
-
почему было принято решение об освобождении крестьян с землей
-
Предмет:
История -
Автор:
kendrick9tjb - 6 лет назад
-
Ответов:
2 -
Смотреть
-
-
План к тексту - описанию весеннего леса. Придумай заголовок.Подбери интересные сравнения , образные выражения, которые ты используешь в своем тексте.
-
Предмет:
Русский язык -
Автор:
deacon26cy - 6 лет назад
-
Ответов:
1 -
Смотреть
-
-
Помогите решить, пожалуйста. ГИА 9 кл.
Дан прямоугольный тр-к АВС. Угол С=90 град., АВ=34, tgA=3/5. Из вершины С проведена высота СН. Найти отрезок ВН.
-
Предмет:
Геометрия -
Автор:
jollyfuentes - 6 лет назад
-
Ответов:
1 -
Смотреть
-
-
точка N лежит на стороне АС правильного треугольника ABC. Найти отношение радиусов окружностей, описаннных около треугольника ABN и ABC, если AN/AC=n
-
Предмет:
Геометрия -
Автор:
paisleykynt - 6 лет назад
-
Ответов:
1 -
Смотреть
-
