-
Пожалуйста помогите решить задачу и написать окислительно- восстановительную реакцию уравнения. Спасибо заранее ❤
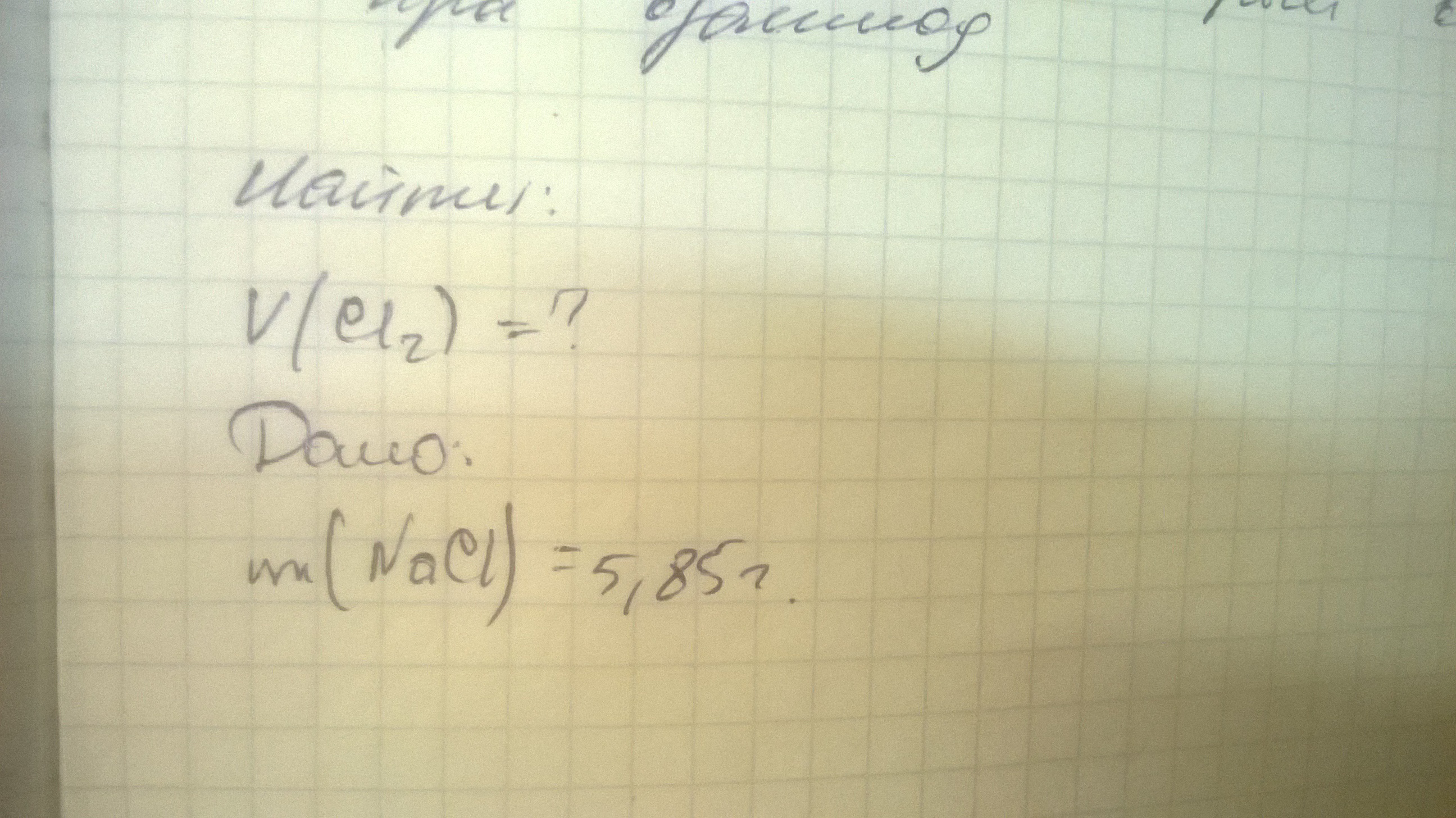
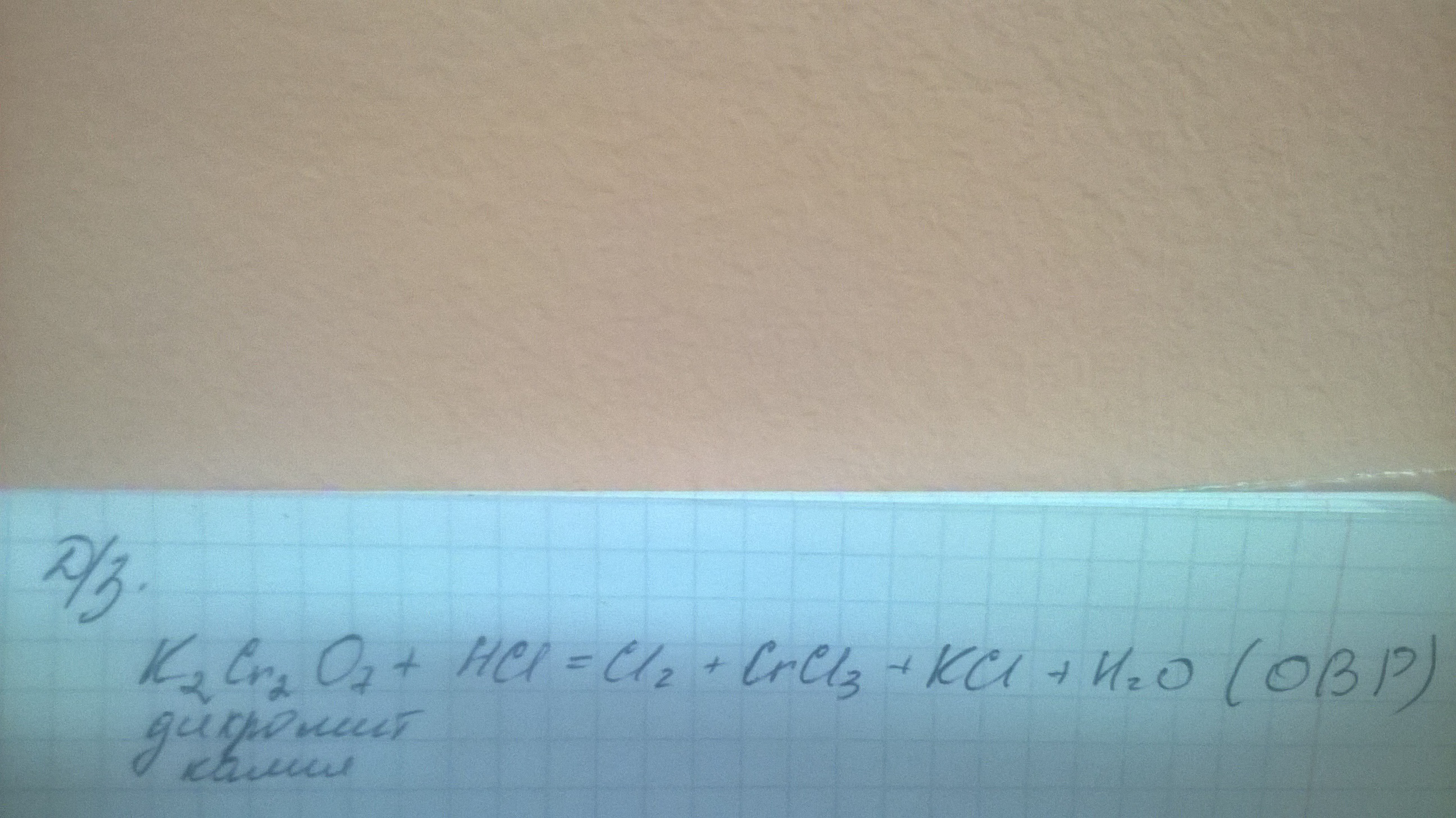
Ответы 1
-
Дано:m(NaCI)=5,85г.Vm=22,4л./моль----------------------------V(CI₂)-?1. Определим молярную массу хлорида натрия и его количество вещества в 5,85г.:M(NaCI)=23+35.5=58.5г./мольn(NaCI)=m(NaCI)÷M(NaCI)=5,85г.÷58,5г./моль=0,1моль.2. Запишем уравнение реакции получения хлора из хлорида натрия:2NaCI + электролиз = 2Na + CI₂3. АНАЛИЗИРУЕМ УРАВНЕНИЕ РЕАКЦИИ:по уравнению реакции из 2моль хлорида натрия образуется 1моль хлора. В условии задачи хлорида натрия 0,1моль, значит хлора получится в два раза меньше: n(CI₂)=0.1моль÷2=0,05моль4. Определим объем хлора:V(CI₂)=n(CI₂) x Vm=0,05моль х 22,4л./моль=1,12л.5. Ответ: из хлорида натрия массой 5,85г. путем электролиза образуется хлор объемом 1,12л.K₂Cr₂⁺⁶O₇ + HCI⁻ ⇒ CI₂⁰ + Cr⁺³CI₃ + KCI + H₂OCr₂⁺⁶ + 3e⁻ ⇒ Cr⁺³ 3 2 Cr₂⁺⁶ окислитель 6 2CI⁻ - 2xe⁻ ⇒ 2CI⁰ 2 3 CI⁻ восстановительK₂Cr₂O₇ + 14HCI = 3CI₂ + 2CrCI₃ + 2KCI + 7H₂O
-
Автор:
gabriel78 - 6 лет назад
-
0
-
-
Добавить свой ответ
Еще вопросы
-
Смена периодов роста и спада производства
-
Тарас и бульба 1,2 глава содержание кратко
-
Предмет:
Литература -
Автор:
giovanizh1d - 6 лет назад
-
Ответов:
1 -
Смотреть
-
-
СРОЧНО ПРЯМО СЕЙЧАС ПОМОГИТЕ ПОЖАЛУЙСТА НОМЕРА 67 и 69 решите хотя бы один номер
-
Предмет:
Математика -
Автор:
kerrydecker - 6 лет назад
-
Ответов:
1 -
Смотреть
-
-
помогите решить уравнения 5 класс z+213=584 300-y=206 t-307=308 166=m-34 59=81-k помогите
-
Предмет:
Математика -
Автор:
dearestifdw - 6 лет назад
-
Ответов:
2 -
Смотреть
-
How much to ban the user?
1 hour
1 day
100 years
