-
помогите, ничего не понимаю в химии
Даже не могу понять, что она написала
темы: "Скорость химических реакций"
"Химическое равновесие"
нужно подробное объяснение
хочу понять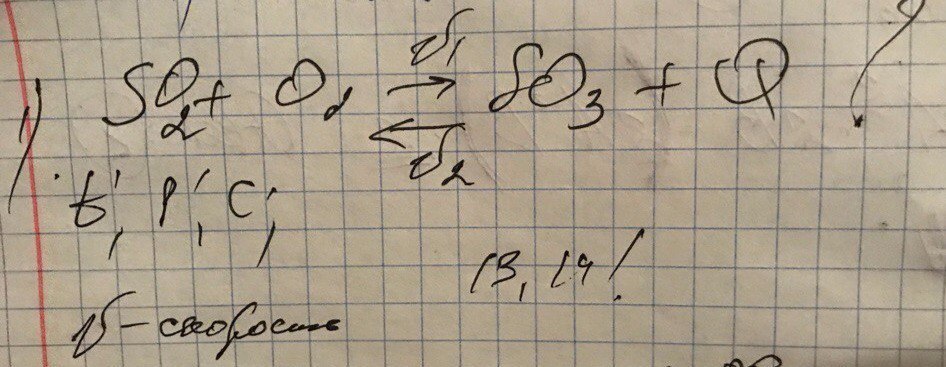
-
Предмет:
Химия -
Автор:
sherleenj2lv - 6 лет назад
-
Ответы 1
-
2SO2+O2=2SO3+Q1)P- давление2моль+1моль=2моль, т.к. считаем только газообразные вещества.При повышении Р химическое равновесие сместится в сторону меньшего объема вещества, т.е. в сторону прямой реакцииПри понижении Р в сторону обратной реакции2) t- температураПри увеличении температуры химическое равновесие смещается в сторону эндотермической реакции, т.е. в сторону обратной реакции При понижении температуры в сторону прямой реакции3) С- концентрацияПри повышении концентрации исходных веществ ( SO2 или О2) химическое равновесие смещается в сторону продуктов, т .е. в сторону прямой реакции. При понижении наоборот.При повышении С продуктов реакции ( SO3) химическое равновесие смещается в сторону исходных веществ, т.е. в сторону обратной реакции
-
Автор:
clarissa - 6 лет назад
-
0
-
-
Добавить свой ответ
Еще вопросы
-
Михаил Пришвин ,,Кот"очень краткое содержание!!Заранее спасибо!!
-
Предмет:
Литература -
Автор:
chewywheeler - 6 лет назад
-
Ответов:
6 -
Смотреть
-
- которая плотность водяного пара при температуре 11 градусов если относительная влажность 80%?
-
на территории трех областей расположено 11.898 озер на терретории кокшетауского региона акмолинской области расположено 1896 озер на терретории северно казахстанской области на л356 озера больше а на терреториии костанайской области все остальные озера сколько озер расположено на территории костанайской области можете составить полноу задачу не только решение
-
Предмет:
Математика -
Автор:
laurarichards - 6 лет назад
-
Ответов:
0 -
Смотреть
-
-
подайте у выгляди многочлена (ax+b²)² , (-1+2c³)²
-
Предмет:
Алгебра -
Автор:
fatimahowell - 6 лет назад
-
Ответов:
1 -
Смотреть
-
How much to ban the user?
1 hour
1 day
100 years
