-
Помогите с окислительно-восстановительными реакциями. Точнее я их решила, но хотелось бы , чтоб вы проверили.Скажите, есть ли ошибки и если да то какой правельный ответ?
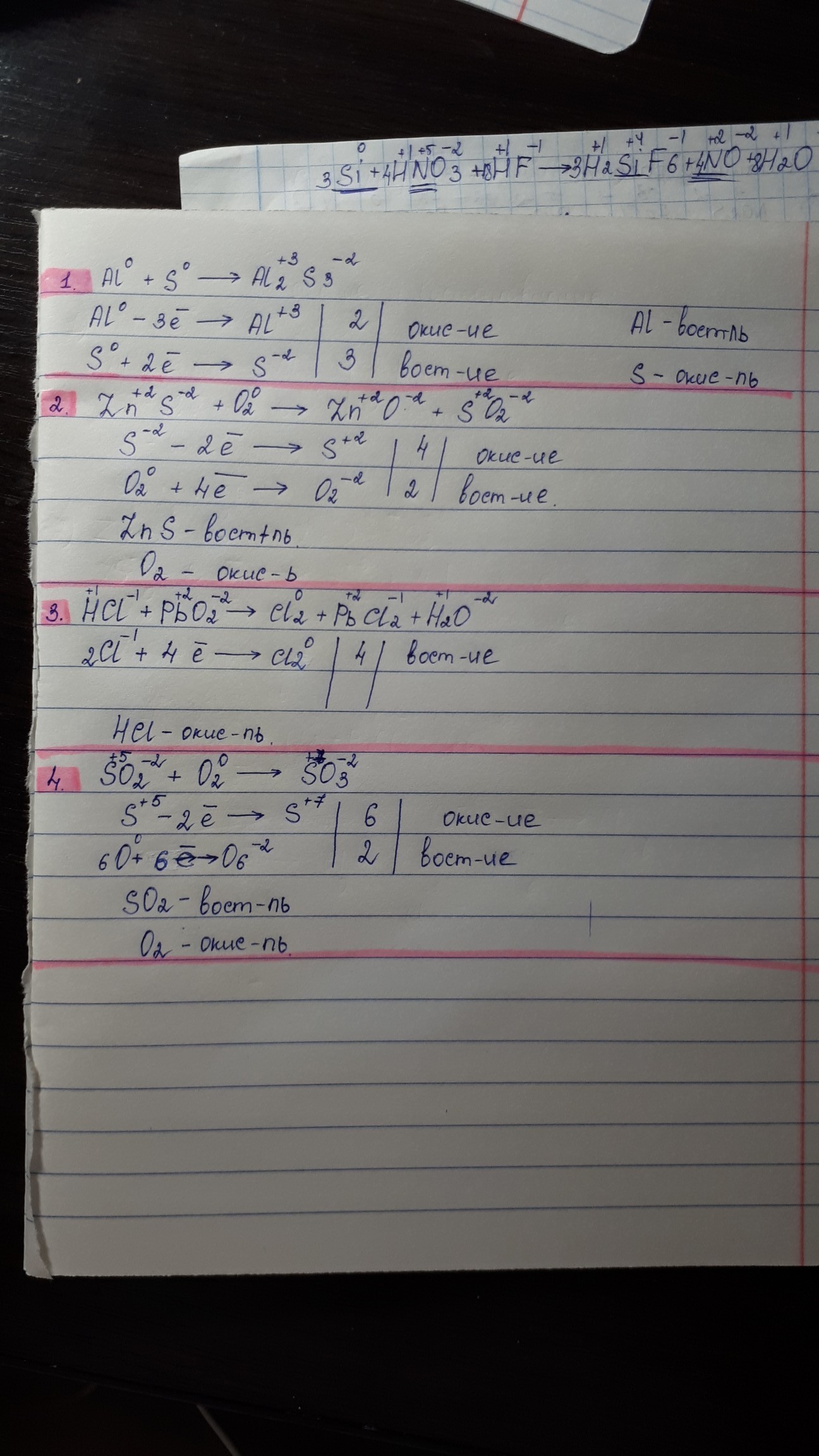
-
Предмет:
Химия -
Автор:
giovanivillarreal - 6 лет назад
-
Ответы 2
-
1. верно, но в уравнении расставить коэф.
2. S -2 в S +4
коэф в электронном балансе ставят перед элементом так что не О2, а из 2О в 2О
3. 2Cl -1→2Cl 0 (-2e)
Pb(+4)→Pb(+2)
4. S(+4)→ S(+6)
-
Автор:
heatherflynn - 6 лет назад
-
0
-
-
Во второй реакции образуется SO2, где у серы степень окисления +4, а не +2 и кислород со степенью -2.
Соответственно, сера будет отдавать 6 электронов, а кислород 4.
В третьем уравнении похожая ошибка. PbO2 - у плюмбума +4, а у кислорода -2. У вас в сумме должно получаться 0. х*1+(-2)*2=0 х-4=0 х=4 Учитывайте индекс
Значит, у плюмбума поменялась степень окисления, записываете схему передачи электронов. Заметьте, что у вас написано только восстановление. Запомните, что всегда должно быть и окисление, и восстановление. Причём количество принятых электронов должно равняться количеству отданных.
В четвертом: откуда у серы +5 и +7? Должно быть +4 и +6. Ещё раз проработайте. В сумме 0.
-
Автор:
slimjuev - 6 лет назад
-
0
-
-
Добавить свой ответ
-
2cosx- корень из 3=0 Найти решение которое принадлежит [-P/2;P/2]
-
Предмет:
Алгебра -
Автор:
skinnymayo - 6 лет назад
-
Ответов:
1 -
Смотреть
-
-
человек,способный сознательно и ответственно
делать выбор-
Предмет:
Обществознание -
Автор:
angelicasoto - 6 лет назад
-
Ответов:
2 -
Смотреть
-
-
Перепишите предложение образуя предложения нереального условия 2 и 3 тип.
If you put on your glasses, you will see better-
Предмет:
Английский язык -
Автор:
nikebrowning - 6 лет назад
-
Ответов:
1 -
Смотреть
-
- Сроооооччнноо. Кто споживає їжі більше слон чи калібрії пояснити
