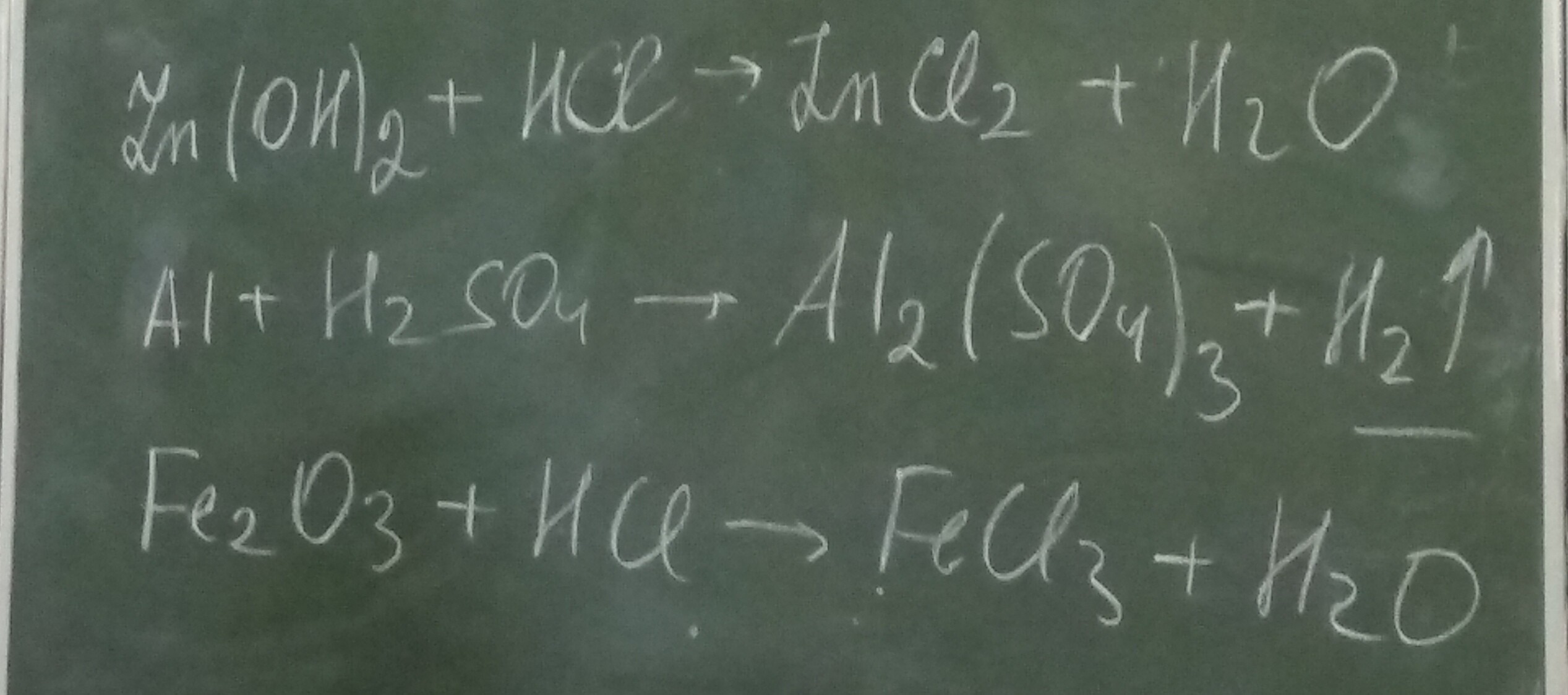Ответы 4
-
Огромное вам спасибо
-
Автор:
cristoferauif - 6 лет назад
-
0
-
-
Текст задач сами составите или составить?
-
Автор:
gromitqeka - 6 лет назад
-
0
-
-
Если не сложно, напишите пожалуйста
-
Автор:
rosahanna - 6 лет назад
-
0
-
-
1. 49,5г. гидроксида цинка взаимодействует с соляной кислотой. Определить массу соляной кислоты.
Дано:
m[Zn(OH)₂]=49,5г.
-------------------------------
m(HCI)-?
Решение:
1. Молярная масса гидроксида цинка:
M[Zn(OH)₂]=65+34=99г./моль
2. Количество вещества гидроксида цинка в 49,5г.:
n₁[Zn(OH)₂] =m[Zn(OH)₂÷M[Zn(OH)₂]
n₁[Zn(OH)₂]=49,5г.÷99г./моль= 0,5моль
3. Zn(OH)₂+2HCI=ZnCI₂+2H₂O
по уравнению реакции:
n( Zn(OH)₂)=1моль n(HCI)=2моль
по условию задачи:
n₁( Zn(OH)₂)=0,5моль n₁(HCI)=1моль
4. Определим молярную массу соляной кислоты:
M(HCI)=36,5г./моль
5. Определим массу соляной кислоты количеством вещества 1моль:
m(HCI)=n₁(HCI)xM(HCI)
m(HCI)=1мольх36,5г./моль=36,5г.
6. Ответ: 36,5г. потребуется соляной кислоты для реакции с 49,5г. гидроксида цинка.
2. Определить объем водорода, образовавшегося при взаимодействии 20г. алюминия с серной кислотой.
Дано:
m(AI)=20г.
Vm=22,4л./моль
--------------------
V(H₂)-?
1.Определим молярную массу алюминия и его количество вещества в 20г.:
M(AI)=27г./моль
n₁(AI)=20г.÷27г./моль=0,7моль
2. Запишем уравнение реакции:
2AI + 3H₂SO₄= AI₂(SO₄)₃ + 3H₂
по уравнению реакции: 2 моль алюминия образуется 3 моль водорода.
по условию задачи: 0,7 моль алюминия образуется 1,05 моль водорода;
n(H₂)=1,05моль
4. Определим объем водорода количеством вещества 1,05 моль :
V(H₂)=n(H₂)xVm=1,05мольx22,4л./моль=23,52л.
5.Ответ: при взаимодействии 20г.алюминия с серной кислотой образовалось 23,52л. водорода.
3. Определить массу хлорида железа(lll), если с оксидом железа(lll) взаимодействует 11,2г. соляной кислоти.
Дано:
m(HCI)=11,2г.
----------------------------------------
m(FeCI₃)-?
Решение:
1. Определим молярную массу его HCI и ее количество вещества количество вещества в 12,1г.:
M(HCI)=36,5г./моль
n(HCI)=m(HCI)÷M(HCI)=12,1г.÷36,5г./моль=0,3моль
2. Запишем уравнение реакции:
Fe₂O₃+6HCI=2FeCI₃+ 3H₂O
по уравнению реакции:
n(Fe₂O₃)=1моль n(FeCI₃) =2моль
по условию задачи:
n₁(Fe₂O₃)=0,3моль n(FeCI₃) =0,6моль
5. Определим молярную массу хлорида железа(lll), его массу количеством вещества 0,3моль:
M(FeCI₃)=56+3х35,5=162,5г./моль
m(FeCI₃)=n(FeCI₃)хM(FeCI₃)=0,3мольх162,5г./моль=48,75г.
7. Ответ: 48,75г. хлорида железа(lll) получится из 11,2г. соляной кислоты.
-
Автор:
harrymaxwell - 6 лет назад
-
0
-
-
Добавить свой ответ
-
Характеристика МАТЕРІ з твору СКАРБ О. Стороженка
-
Предмет:
Українська література -
Автор:
vincent49 - 6 лет назад
-
Ответов:
2 -
Смотреть
-
-
помагите пожалуйста срочно нужнр прошууууууу
составить предложение с 1.полным и неполным
2.двусоставным и односотавным
3.распространенным и нераспространенным
4.простыми и сложными предложениями-
Предмет:
Русский язык -
Автор:
alizahuber - 6 лет назад
-
Ответов:
1 -
Смотреть
-
-
кто нибудь нормально покажет и объяснить мне солнышки??
-
Предмет:
Математика -
Автор:
haylee - 6 лет назад
-
Ответов:
1 -
Смотреть
-
-
Составить ребус к слову линия
-
Предмет:
Русский язык -
Автор:
dorkdcsu - 6 лет назад
-
Ответов:
1 -
Смотреть
-