-
Для предложенного варианта(константы прикреплены)50 баллов за решение:
а) определить стандартное изменение энтальпии химической реакции
(∆ ), зная стандартные энтальпии образования веществ. Определить тип химической реакции (эндо – или экзотермическая реакция);
б) вычислить изменение энтропии химической реакции (∆ );
в) рассчитать значение изобарно-термического потенциала (∆G0(х.р)); (энергии Гиббса) и сделать вывод о возможности самопроизвольного протекания процесса при температуре 298 К.
H2(г) + NO2(г) → NH3(г) + H2O(р)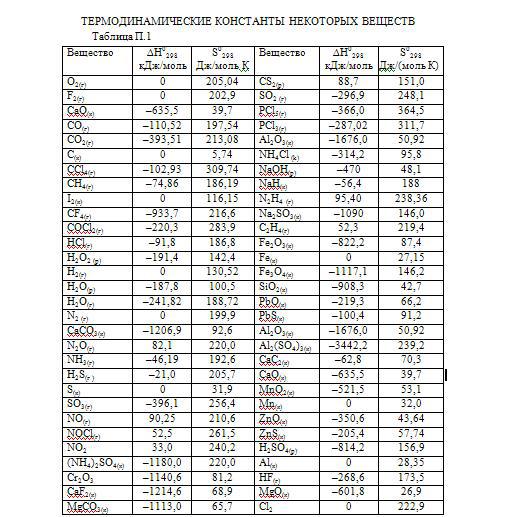
Ответы 1
-
H2(г) + NO2(г) → NH3(г) + H2O(р)1. изменение энтальпии ∆Нреакции= ( ∆Н аммиака (газ) + ∆Н воды (жидкость) ) - (∆Н водорода (газ) + ∆Н оксида азота 4 (газ)) = (-46,19 -187,8) -( 0 +33) = - 299,99 кДж/мольРеакция экзотермическая2. аналогично изменение энтропии ∆S= ∆S продуктов - ∆S реагентов = (192,6+100,5) - (130,52 + 240,2)= - 77,62 Дж/моль3. Изменение энергии Гиббса = -299990 + 298*77,62= - 276,860 кДж/моль реакция самопроизвольно будет идти , т к изменение энергии Гиббса меньше нуля
-
Автор:
mccall - 6 лет назад
-
0
-
-
Добавить свой ответ
Еще вопросы
-
Если открыть одновременно первую и вторую трубы, то пустой бассейн наполнится за 2,5 часа. Одна вторая труба наполняет пустой бассейн за 3,75 часа. За сколько часов наполняет пустой бассейн одна первая труба?
-
Предмет:
Математика -
Автор:
paul86 - 6 лет назад
-
Ответов:
1 -
Смотреть
-
-
"что значит быть духовно богатым человеком" ( сочинение, можно мини)
-
Предмет:
Обществознание -
Автор:
montes - 6 лет назад
-
Ответов:
1 -
Смотреть
-
-
как правильно произносится слово pantry
-
Предмет:
Английский язык -
Автор:
jamiedyer - 6 лет назад
-
Ответов:
7 -
Смотреть
-
-
на столе лежат ложки и вилки:ложек 6,а вилок в 2раза больше.сколько всего ложек и вилок?
-
Предмет:
Математика -
Автор:
eugenio - 6 лет назад
-
Ответов:
1 -
Смотреть
-
How much to ban the user?
1 hour
1 day
100 years
